多巴胺转运体通过摄取多巴胺进入神经元,在多巴胺能神经传递的调节中起着至关重要的作用,并有治疗精神运动兴奋剂滥用的潜力。尽管经过几十年的研究,人类多巴胺转运体的结构、底物结合、构象转变和药物结合姿势仍然未知。2024年8月7日,中国科学院生物物理研究所赵岩团队在Nature在线发表题为“Dopamine reuptake and inhibitory mechanisms in human dopamine transporter”的研究论文,该研究利用单颗粒冷冻电镜技术解析了人源多巴胺转运蛋白DAT未结合底物、结合底物多巴胺、结合治疗ADHD药物哌醋甲酯、结合抑制剂GBR12909以及结合Benztropine的五个高分辨率结构。封闭状态下的多巴胺结合结构精确地说明了多巴胺及其相关离子的结合位置。与药物结合的结构以外向或内向的状态被捕获,阐明了底物运输过程中不同的结合模式和构象转变。与可卡因稳定的外向状态不同,GBR12909和苯托品将多巴胺转运蛋白稳定在内向状态,揭示了以前看不见的药物结合姿势,并为它们如何抵消可卡因的影响提供了见解。该研究为理解人类多巴胺转运体的功能和开发多巴胺转运体相关疾病和可卡因成瘾的治疗干预措施建立了一个框架。可卡因成瘾是一个世界性的公共问题,影响着美国4100多万人。可卡因的运动刺激作用和奖励作用主要源于其对DAT的抑制,导致细胞外多巴胺的快速和过度积累。考虑到多巴胺转运体在可卡因成瘾特性中的关键作用,针对DAT的药物开发代表了从药理学上解决可卡因滥用的逻辑策略。先前的研究表明,尽管GBR12909、苯托品及其衍生物是多巴胺再摄取的有效抑制剂,但它们不会在小鼠和恒河猴中引起类似可卡因的运动活动或自我给药。相反,这些化合物能够减少可卡因的自我给药和可卡因歧视,这表明它们有可能治疗可卡因成瘾。然而,在人类受试者中使用GBR12909的临床研究由于对心室去极化-复极化间隔的速率依赖效应的出现而终止。深入了解这种药物的结合位姿对其进一步优化至关重要。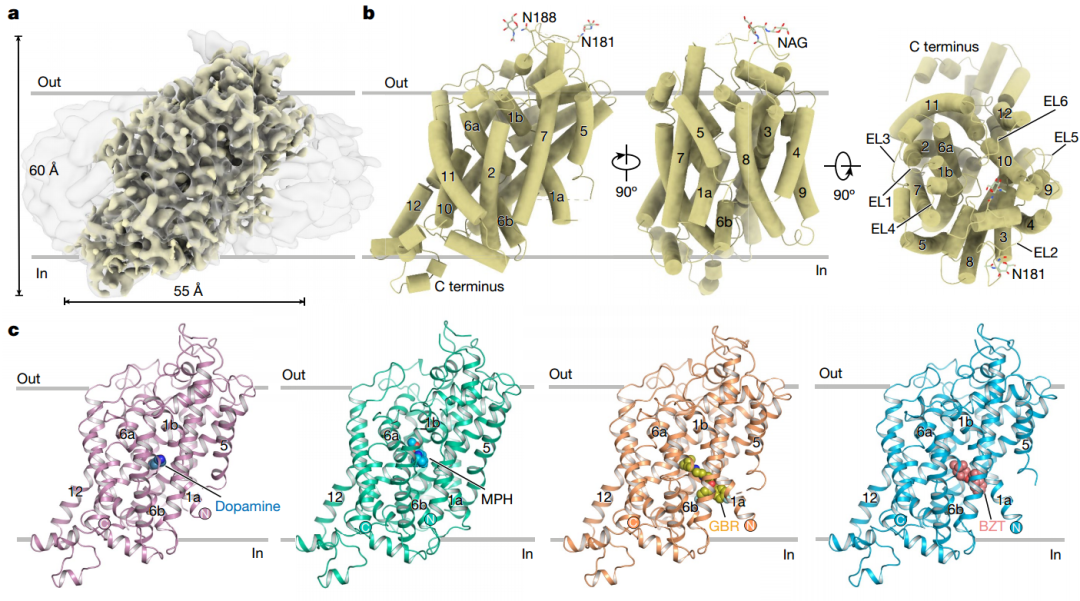
不同配体结合态hDAT的结构(图源自Nature)到目前为止,果蝇DAT (dDAT)的结构已经在底物或各种抗抑郁药的存在下确定,但仅在面向外的状态下。然而,与人类健康和药物开发最相关的hDAT结构尚未确定。此外,促进多巴胺在DAT中的转运的构象变化,特别是在向外、闭塞和内向状态之间的转变,仍然缺乏表征。此外,药物在内向状态下的结合模式尚不清楚,但对于开发有效的药物治疗ADHD和可卡因成瘾具有较少的滥用倾向是可取的。在这项研究中,作者测定了hDAT在载子状态下以及与MPH、GBR12909或苯托品配合物的冷冻电镜结构。这些结构揭示了底物和离子结合口袋,并描绘了不同功能状态之间的构象变化,包括外向、闭塞和内向状态。与药物结合的结构清楚地说明了细胞外和细胞内不同药物分子的结合姿势。这些结构见解为hDAT的生理和药理学机制提供了基础和重要的理解。中国科学院生物物理研究所赵岩研究员为该论文通讯作者,中国科学院生物物理研究所博士研究生李悦、副研究员王先平、博士生孟宇飞、博士生胡拓和北京大学现代农业研究院赵珺研究员为论文的共同第一作者。此外,实验室成员黎仁杰、白秦儒、魏一青、邱云龙、蒿坤、韩君,中国海洋大学博士研究生袁璞和首都医科大学附属北京朝阳医院李娜也为本研究提供了帮助。
论文链接:https://www.nature.com/articles/s41586-024-07796-0
文章转载自微信公众号:广东省心理卫生协会